
Actualité
CIME - Projet immobilier du CHU Grenoble Alpes
Le CHU Grenoble Alpes repensé, au service de chacun CIME, le projet immobilier de modernisation de l’hôpital Michallon, est la concrétisation du...
Lire la suiteAccessibilité
Afin d'être accessible au plus grand nombre, nous vous informons que vous avez la possibilité de
modifier la taille d’affichage du contenu de notre site.
Pour cela, voici les commandes à reproduire à l'aide de votre clavier (sur MAC : remplacer CTRL par CMD) :
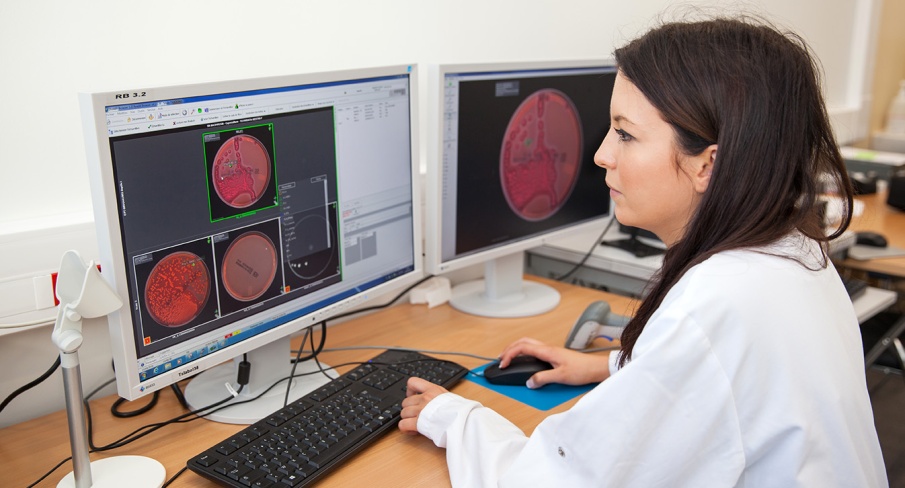
© Ce contenu est mis à disposition par le LEEM.
Un essai clinique est une étude scientifique réalisée en thérapeutique médicale humaine pour évaluer l'efficacité et la tolérance d'une méthode diagnostique ou d'un traitement.
Les personnes malades mais aussi les volontaires sains peuvent participer à un essai clinique, sous réserve des conditions propres à chaque étude.
L’intérêt pour le patient réside dans le fait qu’il participe à un essai innovant dans de bonnes conditions de sécurité. De plus, le patient qui participe à la recherche bénéficie d’un meilleur suivi médical et d’un accès à un traitement avant sa commercialisation. A savoir que pour bénéficier d’un traitement innovation, en moyenne, il faut 3 à 4 années avant sa commercialisation.
Pour les volontaires se prêtant à la recherche, l’intérêt est avant tout de faire avancer la recherche et de s’engager pour la santé et la qualité de vie de la collectivité.
Malade ou en bonne santé, nous avons tous un jour ou l’autre besoin d’un médicament ou d’une thérapie innovante. Et sans essai clinique, nous n’aurions pas accès aux médicaments et aux innovations dans les conditions optimales de sécurité.
Il y a trois raisons principales :
La recherche clinique constitue un enjeu de compétition mondiale. Elle favorise les investissements en santé sur le territoire français et peut être source d’emplois très qualifiés.
Il est important de souligner que la France est un grand pays dans le domaine de la recherche clinique et se place au 5ème rang mondial des essais cliniques en oncologie en 2020.
A l’origine de toute étude clinique, il y a un promoteur, c’est-à-dire une personne physique ou morale qui porte la responsabilité de l’étude et qui en assure le financement et la réalisation.
Une fois le protocole de l’essai établi, le promoteur demande l’autorisation de réaliser l’essai à l’Agence Nationale de Sécurité du Médicament (ANSM) et en parallèle, ce même protocole est envoyé à un Comité de Protection des Personnes (CPP) qui s’assure que la protection des participants à la recherche est assurée. Une fois autorisé, avec un avis favorable du CPP, l’essai peut démarrer.
Pour un essai randomisé, plusieurs groupes de personnes sont traités en parallèle par des médicaments dont on souhaite comparer les effets. Certains participants reçoivent le médicament test, d’autre un médicament existant ou d’autres encore un placebo. C’est un tirage au sort informatisé, la randomisation, qui constitue les différents groupes.
Les médecins qui dirigent et surveillent la réalisation des essais cliniques sont appelés les « investigateurs ». Le patient voit régulièrement le médecin investigateur qui suit aussi immédiatement tout effet indésirable qui pourrait survenir au cours de l’essai.
L’investigateur s’assure du bon déroulement de la recherche, dans le respect des bonnes pratiques cliniques.
A l’issue d’un essai clinique, les malades qui ont été inclus continuent à être suivis par une équipe médicale.
Tous les essais cliniques doivent être répertoriés dans un registre et les résumés des résultats publiés pour les patients un an après la fin de l’essai. On peut consulter le résumé des résultats sur Internet : clinicaltrials.gov et clinicaltrialsregister.eu
En France, la législation a été l’une des premières mises en place en Europe assurant la protection des patients inclus dans les essais.
Un essai clinique ne peut se dérouler que s’il y a une autorisation de l’Agence Nationale de Sécurité du Médicament (ANSM) et un avis favorable du Comité de Protection des Personnes (CPP). L’ANSM assure également le suivi de la sécurité des essais tout au long de leur déroulement.
L’information des patients est un élément capital de la protection des personnes. Cette information est validée par le CPP.
Toute personne qui participe à un essai clinique doit signer un document dit de consentement éclairé. Ce document garantit que le patient a reçu de la part du médecin investigateur toutes les informations nécessaires sur les objectifs, la méthodologie, la durée de la recherche, les bénéfices attendus, les contraintes et les risques prévisibles ou encore la possibilité de retirer son consentement à tout moment et sans préjudice. Ainsi aucun essai ne peut se faire sans le consentement libre, éclairé et écrit du patient.
Le patient n’est jamais seul, il peut quitter un essai clinique quand il le désire et continuera à être suivi par les médecins. De fait, les essais sont très encadrés et les patients bien suivis.
Le CHU Grenoble Alpes souhaite entreprendre les projets ci-dessous sur des données et/ou échantillons biologiques existants.
Aucun nouveau prélèvement ne sera effectué, aucune nouvelle visite au CHU ne sera nécessaire, et aucun questionnaire ne vous sera envoyé.
Le traitement des données est réalisé par le CHUGA (responsable de traitement) et a pour fondement les articles 6 (mission d’intérêt public) et 9 (traitement de données de santé à des fins de recherche scientifique) du règlement UE 2016/679 (Règlement Général sur la Protection des Données (RGPD)).
Les données seront traitées en conformité avec les directives de la CNIL pour assurer la sécurité de vos données personnelles et la conformité avec le règlement européen sur la protection des données (RGPD). Aussi :
Cette page vous concerne si vous avez été patient au CHUGA et que vous avez été informé de la réutilisation possible de vos données de soins pour des projets de recherche.
Si vous êtes opposé à l’utilisation de vos données personnelles ou à l'utilisation de vos échantillons, pour l’un de ces projets, ou si vous avez besoin d’informations supplémentaires, vous pouvez contacter le délégué à la protection des données du CHUGA par l’un de ces moyens, ou bien lui envoyer ce formulaire d'opposition rempli :
Les données sont stockées de manière sécurisée et avec des modalités d’accès contrôlées jusqu’à deux ans après la dernière publication des résultats de la recherche ou, en cas d’absence de publication, jusqu’à la signature du rapport final de la recherche.


Actualité
CIME - Projet immobilier du CHU Grenoble Alpes
Le CHU Grenoble Alpes repensé, au service de chacun CIME, le projet immobilier de modernisation de l’hôpital Michallon, est la concrétisation du...
Lire la suite
Actualité
Retour sur l'année 2024 au CHUGA
L’année 2024 a été marquée par des réalisations significatives, fruit de l’engagement et de l’énergie collective de toutes les équipes. Revenons...
Lire la suite
Actualité
Le CHU Grenoble Alpes s’engage contre les violences sexistes et sexuelles, et les discriminations
Le CHU Grenoble Alpes (CHUGA) renforce son engagement en faveur d’un environnement de travail respectueux et inclusif en lançant une campagne de...
Lire la suite
Actualité
Exposition - Enfanter, une évolution des pratiques à l’hôpital de Grenoble
Enfanter, une évolution des pratiques à l’hôpital de Grenoble Exposition ouverte ! Après « Cousu main », une exposition qui retraçait les...
Lire la suite
Actualité
Semaine nationale de la continence
Semaine nationale de la continence - Campagne de l'AFU En finir avec les "envies pressantes" Jeudi 20 mars - 18h30 : Rendez-vous Live sur le compte...
Lire la suite
Actualité
Port du masque obligatoire
Dans le contexte de circulation importante des virus respiratoires (grippe, COVID-19, virus respiratoires), le port de masque chirurgical est...
Lire la suite
Actualité
Régulation des admissions aux urgences
Lire la suite

Actualité
Aidez à former les soignants de demain !
Dans le cadre de notre mission d’enseignement, nous formons chaque année près de 1500 étudiants au sein de nos écoles et instituts de formation. En...
Lire la suite
Actualité
Et si ta place était avec nous ?
De nombreux métiers sont à ta portée au sein de notre établissement, consulte nos offres d'emplois dès maintenant ! 100 métiers différents, un même...
Lire la suite
Actualité
Le Fonds de dotation du CHUGA
Aux côtés des soignants, au bénéfice des patients !
Lire la suite
Actualité
Le CHU Grenoble Alpes certifié « Haute Qualité des Soins » par la Haute Autorité de Santé
Après avoir été en 2019 le premier CHU français à être certifié de niveau A dans sa globalité et en première intention par le collège de la Haute...
Lire la suite